


近日,Phathom Pharmaceuticals宣布,美国FDA已批准Voquezna Triple Pak(伏诺拉生,阿莫西林,克拉霉素三重组合)和Voquezna Dual Pak(伏诺拉生,阿莫西林双重组合)上市,用于治疗成人幽门螺杆菌(Helicobacter pylori)感染。新闻稿指出,这两种组合均包含伏诺拉生,这是一款“first-in-class” 钾离子竞争性酸阻滞剂,是美国30多年来批准的首款源于新药物类型的创新抑酸疗法。
全球约50%的人口受到幽门螺杆菌感染。幽门螺杆菌感染激发的慢性炎症,可导致感染者出现一系列疾病,包括消化不良、消化性溃疡病、胃癌和粘膜相关淋巴组织(MALT)淋巴瘤。抑酸疗法一直是幽门螺杆菌感染治疗方案的支柱之一,它可以增强抗生素的效果。更强力的抑酸药物(比如伏诺拉生),可能提高目前治疗方案的根除率。
伏诺拉生☚是一款新型钾离子竞争性酸阻滞剂(P-CAB),可以竞争性阻滞钾离子与氢/钾离子ATP酶的结合,从而快速抑制胃酸的分泌。由于伏诺拉生半衰期长,作用时间更持久,因此被视为一种有效的长效质子泵抑制剂(PPI)。FDA此前已授予vonoprazan三重和双重组合疗法合格传染病产品资格(QIDP)和快速通道资格,用于治疗幽门螺杆菌感染。
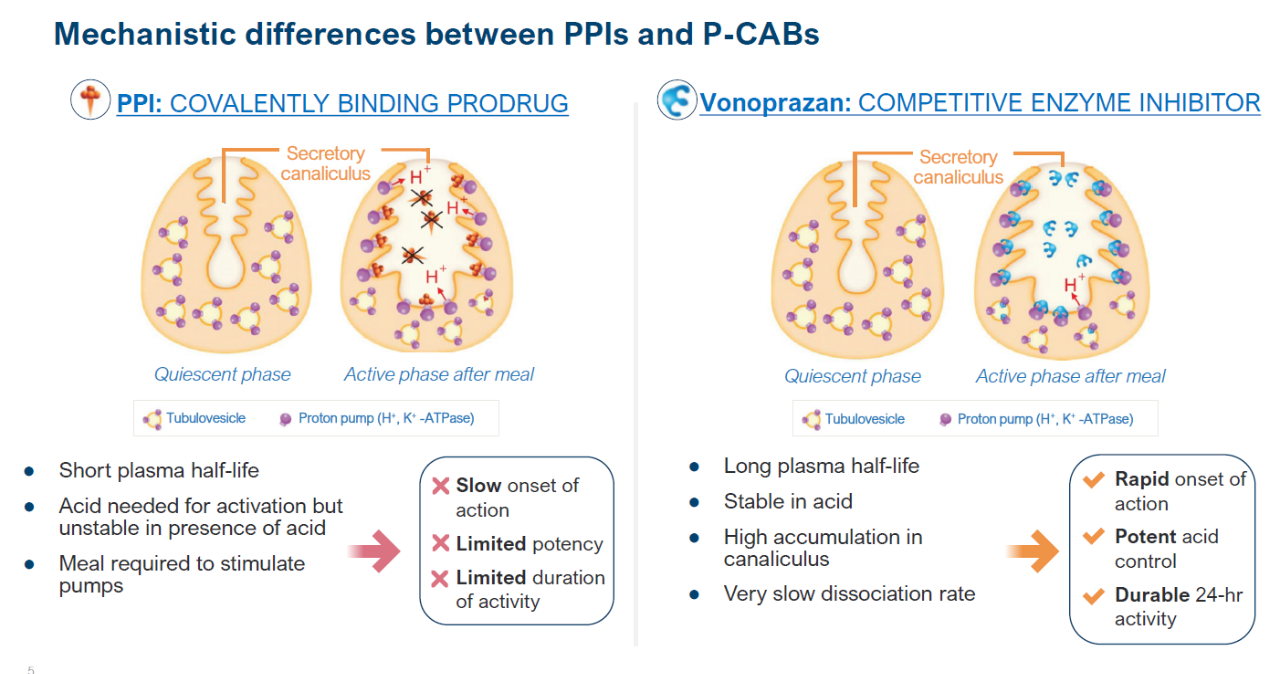
▲伏诺拉生具有独特的作用机制(图片来源:Phathom Pharmaceuticals官网)
FDA的批准是基于一项包含1046名患者的关键性3期临床试验的结果。试验结果显示,伏诺拉生三重和双重组合疗法达到试验的主要终点,与基于兰索拉唑(lansoprazole)的三重组合疗法相比,根除率达到非劣效性标准。在改良的意向治疗人群(mITT)中,伏诺拉生三重组合的根除率为84.7%,双重组合的根除率为78.5%,兰索拉唑三重组合疗法根除率为78.8%。
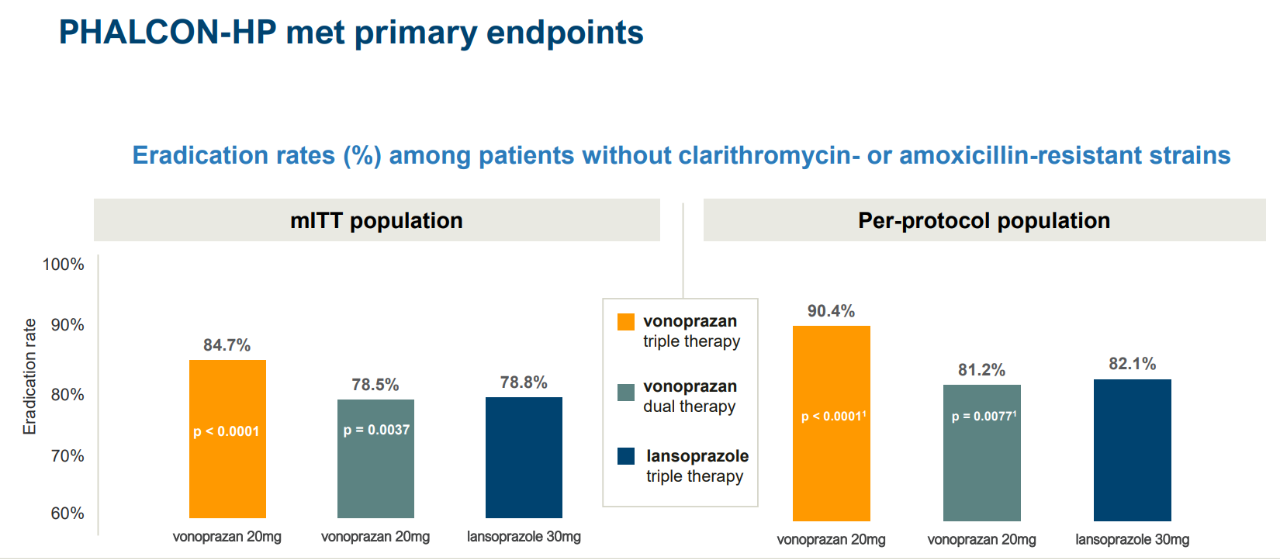
▲伏诺拉生组合疗法达到3期临床试验主要终点(图片来源:Phathom Pharmaceuticals官网)
在包含被克拉霉素耐药性幽门螺杆菌感染的全部患者人群中,伏诺拉生三重组合的根除率为80.8%,双重组合疗法为77.2%,均优于兰索拉唑三重组合疗法(68.5%)。
“Voquezna治疗方案的获批给医生和患者两种治疗选择。它们在关键性临床试验中与基于质子泵抑制剂兰索拉唑的组合疗法相比,在全部患者人群中表现出更优的根除率。”Phathom总裁兼首席执行官Terrie Curran女士说,“幽门螺杆菌根除率由于抗生素耐药性,抑酸水平不足,以及治疗方案复杂等原因不断下降。患者需要解决现有疗法局限的新疗法,我们期待将基于伏诺拉生的治疗选择带给上百万幽门螺杆菌感染者。”
参考资料:
[1] Phathom Pharmaceuticals Announces FDA Approval of VOQUEZNA™ TRIPLE PAK™ (vonoprazan, amoxicillin, clarithromycin) and VOQUEZNA™ DUAL PAK™ (vonoprazan, amoxicillin) for the Treatment of H. pylori Infection in Adults. Retrieved May 3, 2022, from https://www.globenewswire.com/news-release/2022/05/03/2435147/0/en/Phathom-Pharmaceuticals-Announces-FDA-Approval-of-VOQUEZNA-TRIPLE-PAK-vonoprazan-amoxicillin-clarithromycin-and-VOQUEZNA-DUAL-PAK-vonoprazan-amoxicillin-for-the-Treatment-of-H-pylo.html
 公安机关备案号:43011102001342 互联网药品信息服务资格证书:(湘)-经营性-2023-0166号
公安机关备案号:43011102001342 互联网药品信息服务资格证书:(湘)-经营性-2023-0166号